Pengertian Gas Ideal Berikut Persamaannya
Apakah Anda pernah mendengar istilah gas sejati dan gas ideal? Keduanya sering dibahas dalam fisika, khususnya dalam termodinamika, karena memiliki peran penting dalam memahami sifat-sifat gas. Meskipun serupa, gas sejati dan gas ideal memiliki perbedaan mendasar yang penting untuk diketahui. Artikel ini akan menjelaskan pengertian gas ideal, sifat-sifatnya, hukum yang terkait, serta persamaan yang digunakan untuk memodelkannya.
Apa Itu Gas Ideal dan Gas Sejati?
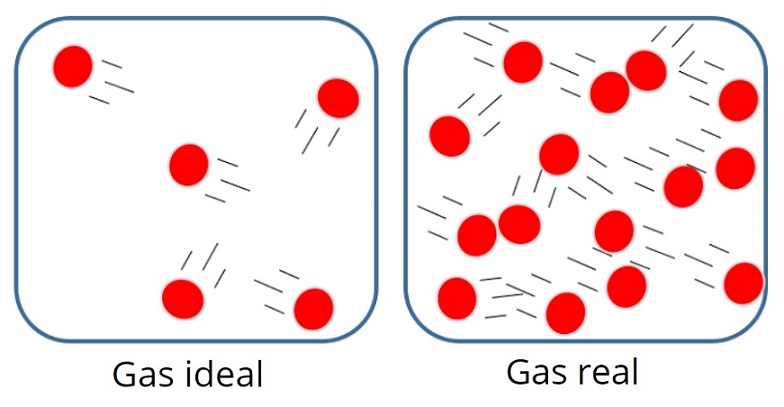
Gas sejati adalah gas nyata yang kita jumpai dalam kehidupan sehari-hari. Contoh gas sejati meliputi udara yang kita hirup, gas karbon dioksida yang dihasilkan dari pembakaran, atau gas metana yang digunakan sebagai bahan bakar. Gas sejati memiliki sifat kompleks karena molekul-molekulnya berinteraksi satu sama lain melalui gaya tarik-menarik atau gaya tolak-menolak. Selain itu, gas sejati juga dipengaruhi oleh berbagai faktor seperti tekanan, suhu, dan volume.
Di sisi lain, gas ideal adalah konsep teoretis yang digunakan untuk menyederhanakan pemahaman tentang perilaku gas sejati. Dalam model gas ideal, interaksi antar molekul dianggap tidak ada, sehingga gas ini tidak dipengaruhi oleh gaya tarik-menarik atau gaya tolak-menolak. Gas ideal adalah model matematika yang mempermudah perhitungan sifat-sifat gas sejati, terutama dalam kondisi tertentu seperti tekanan rendah atau suhu tinggi.
Pengertian Gas Ideal Berikut Persamaannya
Sifat-Sifat Gas Ideal
Gas ideal dirancang dengan asumsi tertentu yang membuatnya lebih mudah dipelajari dibandingkan gas sejati. Berikut adalah beberapa sifat utama gas ideal:
Molekul Gas Tidak Berinteraksi
Dalam gas ideal, tidak ada gaya tarik-menarik atau gaya tolak-menolak antar molekul. Hal ini berarti molekul bergerak bebas tanpa dipengaruhi molekul lainnya.
Molekul Berukuran Sangat Kecil
Molekul gas ideal dianggap sebagai titik materi dengan volume yang sangat kecil dibandingkan dengan volume total gas. Dengan asumsi ini, volume molekul gas dapat diabaikan.
Tumbukan Elastis
Ketika molekul gas bertumbukan, baik dengan dinding wadah maupun molekul lain, tumbukan tersebut dianggap slot deposit 5000 elastis sempurna. Artinya, tidak ada kehilangan energi kinetik selama tumbukan.
Gerak Acak
Molekul gas ideal selalu bergerak secara acak dan konstan dalam segala arah. Kecepatan molekul-molekul ini dipengaruhi oleh suhu gas.
Energi Kinetik Sebanding dengan Suhu
Energi kinetik rata-rata molekul gas ideal hanya bergantung pada suhu gas tersebut. Hubungan ini mengikuti prinsip kinetika gas.
Hukum yang Berlaku pada Gas Ideal
Gas ideal mengikuti beberapa hukum dasar yang menggambarkan hubungan antara tekanan, volume, suhu, dan jumlah molekul gas. Berikut adalah tiga hukum utama yang sering digunakan:
Hukum Boyle
Menyatakan bahwa pada suhu tetap, tekanan gas berbanding terbalik dengan volumenya. Secara matematis, dirumuskan sebagai:
𝑃
×
𝑉
=
konstan
P×V=konstan
di mana
𝑃
P adalah tekanan dan
𝑉
V adalah volume.
Hukum Charles
Pada tekanan tetap, volume gas berbanding lurus dengan suhu absolutnya:
𝑉
∝
𝑇
V∝T
atau
𝑉
1
𝑇
1
=
𝑉
2
𝑇
2
T
1
V
1
=
T
2
V
2
dengan
𝑇
T adalah suhu dalam Kelvin.
Hukum Avogadro
Hukum ini menyatakan bahwa pada tekanan dan suhu tetap, volume gas sebanding dengan jumlah mol gas:
𝑉
∝
𝑛
V∝n
di mana
𝑛
n adalah jumlah mol gas.
Persamaan Gas Ideal
Semua hukum di atas dirangkum dalam persamaan gas ideal, yang merupakan dasar dalam mempelajari termodinamika gas. Persamaan ini dinyatakan sebagai:
𝑃
×
𝑉
=
𝑛
×
𝑅
×
𝑇
P×V=n×R×T
di mana:
𝑃
P: tekanan gas (Pa)
𝑉
V: volume gas (m³)
𝑛
n: jumlah mol gas
𝑅
R: konstanta gas ideal (8,314 J/mol·K)
𝑇
T: suhu gas (K)
Persamaan ini sangat berguna untuk memprediksi perilaku gas dalam berbagai kondisi.
Kapan Gas Sejati Mendekati Gas Ideal?
Meskipun gas sejati jarang sepenuhnya memenuhi asumsi gas ideal, ada kondisi tertentu di mana gas sejati dapat mendekati sifat-sifat gas ideal, yaitu:
Tekanan Rendah
Pada tekanan rendah, jarak antar molekul gas menjadi lebih besar, sehingga interaksi antar molekul dapat diabaikan.
Suhu Tinggi
Pada suhu tinggi, energi kinetik molekul gas jauh lebih besar dibandingkan dengan gaya tarik-menarik antar molekul, membuat perilaku gas sejati menyerupai gas ideal.
Penutup
Gas ideal adalah model teoretis yang mempermudah pemahaman tentang sifat dan perilaku gas sejati. Dengan asumsi-asumsi yang menyederhanakan, model gas ideal digunakan untuk memprediksi hubungan antara tekanan, volume, suhu, dan jumlah molekul gas. Meskipun gas sejati tidak sepenuhnya memenuhi asumsi gas ideal, konsep ini tetap relevan, terutama dalam kondisi tekanan rendah dan suhu tinggi. Memahami perbedaan dan hubungan antara gas sejati dan gas ideal menjadi langkah penting dalam mempelajari fisika termodinamika.